Ce determină culoarea focului? De ce focul este de culori diferite, ce determină culoarea flăcării
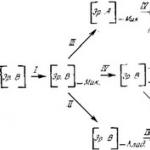
Aprindeți o lumânare și examinați îndeaproape flacăra. Veți observa că nu este uniformă la culoare. Flacăra are trei zone (fig.). Zona întunecată 1 este în partea de jos a flăcării. Aceasta este cea mai rece zonă în comparație cu altele. Zona întunecată este mărginită de partea cea mai strălucitoare a flăcării 2. Temperatura este mai mare decât în zona întunecată, dar cea mai ridicată temperatură este în partea superioară a flăcării 3.
Pentru a te asigura că zone diferite flăcări au temperaturi diferite, puteți efectua un astfel de experiment. Puneți așchia (sau chibritul) în flacără, astfel încât să traverseze toate cele trei zone. Veți vedea că pata este mai carbonizată acolo unde a intrat în zonele 2 și 3. Aceasta înseamnă că flacăra este mai fierbinte acolo.
La toate răspunsurile voi adăuga încă un detaliu care este folosit de chimiști. Există mai multe zone în structura flăcării. Cea care este interioară, albastră, cea mai rece (față de alte zone) este așa-numita flacără de reducere. Acestea. poate efectua reacții de reducere (de exemplu, oxizi de metal). Top parte Galben-roșu este zona cea mai fierbinte, numită și flacără oxidantă. În ea are loc oxidarea vaporilor de materie cu oxigenul atmosferic (dacă, desigur, vorbim despre o flacără obișnuită). Poate efectua reacțiile chimice adecvate.
Culoarea focului depinde de elementele chimice care ard în timpul arderii, de exemplu, dacă vrei să vezi o lumină albastră, atunci apare atunci când arde gazul natural și este cauzată de monoxidul de carbon, care dă această nuanță. Flăcări galbene apar atunci când sărurile de sodiu se descompun. Lemnul este bogat în astfel de săruri, deci un incendiu de pădure obișnuit sau chibrituri de uz casnic arde cu o flacără galbenă. Cuprul dă flăcări nuanță verde... Cu un conținut ridicat de cupru în materialul combustibil, flacăra are o lumină strălucitoare Culoarea verde aproape identic cu albul.
Bariul, molibdenul, fosforul, antimoniul dau, de asemenea, culoarea verde și nuanțele sale la foc. Seleniul colorează flacăra în albastru, iar borul în albastru-verde. O flacără roșie va da litiu, stronțiu și calciu, potasiu violet, o nuanță galben-portocalie iese când sodiul este ars.
Ei bine, dacă cineva este interesat de mai multe informatii detaliate consultați această pagină http://allforchildren.ru/why/misc33.php
culoarea flăcării depinde de temperatura acesteia, precum și de compoziția substanței care arde:
4300K - alb și galben, cea mai strălucitoare lumină;
5000K - rece culoare alba;
6000K - alb cu albastru deschis
8000K - albastru-cian - calitatea luminii este mai proasta.
12000K violet
Deci, de fapt, cea mai fierbinte flacără de lumânare este de jos, nu de sus, așa cum a spus Maxim 26ru 325, iar temperatura la vârful flăcării este mai mare doar datorită prezenței gravitației pe Pământ - curenții de convecție apar ca rezultatul căruia căldura se repezi vertical în sus.
Culoarea focului depinde direct de temperatura flăcării, iar temperatura, la rândul ei, eliberează o substanță, care va da o anumită culoare în spectrul său. De exemplu:
Curmalele carbohidrate sunt albastre;
Bor - Albastru-verde;
Culoarea galben-portocalie este emisă de sărurile de sodiu
Culoarea verde provine din eliberarea de cupru, molibden, fosfor, bariu, antimoniu
Albastrul este seleniu
Roșu din eliberarea de litiu și calciu
Curmale mov potasiu
La început, așa cum a spus Alexander Antipov - da, culoarea flăcării este determinată de temperatura acesteia (dacă nu mă înșel, a fost dovedit de Planck). Și apoi materialul care arde se acumulează în flacără. Atomii diferitelor elemente sunt capabili să absoarbă cuante cu o anumită energie și să le emită înapoi, dar cu o energie care depinde de natura atomului. Galbenul este culoarea sodiului într-o flacără. Sodiul se găsește în orice natură material organic... A galben capabil să înece alte culori - aceasta este o caracteristică a vederii umane.
Ei bine, depinde ce fel de foc. Poate fi de orice culoare, în funcție de substanța care arde. Și o astfel de flacără albastră-gălbuie de la încălzirea ei. Cu cât flacăra este mai departe de substanța care arde, cu atât este mai mult oxigen. Și cu cât mai mult oxigen, cu atât flacăra este mai fierbinte și, prin urmare, mai ușoară și mai strălucitoare.
În general, temperatura din interiorul flăcării este diferită și în timp se modifică (în funcție de fluxul de oxigen și de o substanță combustibilă). Culoarea albastraînseamnă că temperatura este foarte ridicată până la 1400 C, galben - temperatura este puțin mai mică decât atunci când este flacăra albastră.
Culoarea flăcării se poate schimba în funcție de impuritățile chimice.
Pagina 1
Culoarea galbenă a flăcării se datorează atomilor de N3 (X 0 589 microni), culoarea albă se datorează prezenței BaO și M § O.
Introducerea unui cristal de sare de azotat de sodiu în flacără produce o flacără galbenă.
Metoda este foarte sensibilă: minimul de deschidere este egal cu 0,0001 y - Prin urmare, prezența sodiului poate fi apreciată numai dacă culoarea galbenă a flăcării este strălucitoare și nu dispare timp de 10 - 15 secunde.
Aprinderea generatorului de gaz se termină la robinetul de testare la șemineu gazul va arde constant cu o flacără uniformă Violet cu o tentă roz. O flacără galbenă indică o calitate slabă a gazului, iar limbi roșii, ușor fumurii, indică gudron în gaz. Dacă calitatea gazului este satisfăcătoare, acesta conține mai puțin de 0 5 - 0 6% oxigen. Dacă gazul nu arde deloc sau clipește și se stinge, atunci acest lucru indică temperatura scazutaîn miez; este necesar să se aprindă mai puternic gazeificatorul.
Acest tip de concluzie nu este perfect. În primul rând, culoarea galbenă a flăcării poate ascunde culoarea flăcării cauzată de alte elemente, iar în al doilea rând, culoarea galbenă poate fi cauzată de impuritățile compușilor de sodiu conținute în analitul principal.
Metoda este foarte sensibilă: minimul de deschidere este de 0,0001 μg. Prin urmare, prezența sodiului poate fi concluzionată numai dacă culoarea galbenă a flăcării este strălucitoare și nu dispare în 10 - 15 secunde.
Pentru a curăța firele, acestea sunt furnizate cu o perlă de borax, care este încălzită, așa cum este indicat în Fig. 2, a, doar pe o parte; în timp ce mingea se mișcă înăuntru partea opusă de-a lungul firului de platină și dizolvă toate impuritățile acestuia din urmă. După repetarea acestei tehnici de trei ori, firul va fi curățat de toate materii străine, cu excepția unei cantități nesemnificative de sticlă care aderă la el, care la rândul său poate fi îndepărtată dacă firul este calcinat în partea de flacără cu cea mai mare temperatura până când culoarea galbenă a flăcării de sodiu dispare complet.
Culoarea galbenă a flăcării, cauzată de urme de săruri de sodiu, maschează adesea flacăra violetă a potasiului. În acest caz, flacăra trebuie privită printr-o prismă de sticlă cu o soluție indigo care absoarbe partea galbenă a spectrului.
Potențialele (energiile) de ionizare ale metalelor alcaline și alcalino-pământoase sunt foarte mici, prin urmare, atunci când un metal sau compusul său este introdus în flacăra arzătorului, elementul este ușor ionizat, colorând flacăra într-o culoare corespunzătoare liniei sale de excitație spectrală. Culoarea galbenă a flăcării este tipică pentru compușii de sodiu, violet pentru compușii de potasiu, roșu cărămidă pentru compușii de calciu.
Atunci de ce sârma de fier dă aceeași lumină? Curățând cu atenție suprafața sârmei de fier, puteți arăta că culoarea galbenă a flăcării nu se datorează fierului; culoarea galbenă se datorează prezenței unor cantități mici de sare pe suprafața sârmei de fier, care este captată de degete, pe care sunt mereu urme de sare. Culoarea galbenă a flăcării este o probă foarte sensibilă la prezența sodiului. Ochiul poate detecta o modificare a colorării flăcării rezultată din introducerea unui element în flacără într-o cantitate semnificativ mai mică de 1 microgram. Găsirea unei cantități atât de mici dintr-o substanță fără această metodă cu flacără este departe de a fi o sarcină ușoară pentru un chimist.
| O parte a diagramei nivelului de energie a electronilor de valență ai atomului de sodiu. Termenul simbol este o desemnare numerică a diferitelor niveluri de energie. Numerele de pe liniile drepte indică lungimile de undă corespunzătoare în nanometri. |
În fig. 2 - 1, în conformitate cu conceptele general acceptate, sunt prezentate unele niveluri de energie ale electronilor exteriori ai unui atom de sodiu neutru. Un electron excitat tinde să revină la starea sa normală (3s); la revenirea la normal, se emite un foton. Fotonul emis are o anumită cantitate de energie, determinată de locația nivelului de energie. În exemplul prezentat, radiația emisă dă naștere la culoarea galbenă familiară a unei flăcări de sodiu și a unei lămpi de sodiu.
Pagini: 1
Flacăra se întâmplă culoare diferita... Privește în șemineu. Flăcări galbene, portocalii, roșii, albe și albastre dansează pe bușteni. Culoarea sa depinde de temperatura de ardere și de materialul combustibil. Pentru a vizualiza acest lucru, imaginați-vă o spirală aragaz electric... Dacă țigla este oprită, spiralele sunt reci și negre. Să presupunem că ai decis să încălziți supa și ați pornit plita. La început, spirala devine roșu închis. Cu cât temperatura crește mai mult, cu atât culoarea roșie a spiralei este mai strălucitoare. Când țigla se încălzește până la temperatura maxima, spirala devine portocaliu-rosu.
Desigur, spirala nu arde. Nu poți vedea flacăra. Ea este foarte fierbinte. Dacă îl încălzești mai mult, atunci și culoarea se va schimba. La început, culoarea spiralei va deveni galbenă, apoi albă, iar când va deveni și mai fierbinte, o strălucire albastră va emana din ea.

Ceva similar se întâmplă cu flăcările. Luați o lumânare de exemplu. Diverse site-uri flăcările lumânărilor au temperaturi diferite. Focul are nevoie de oxigen. Dacă acoperi lumânarea Borcan de sticlă, focul se va stinge. Centrul, adiacent fitilului, al flăcării lumânării consumă puțin oxigen și arată întunecat. Partea superioară și părțile laterale ale flăcării primesc mai mult oxigen, astfel încât aceste zone sunt mai luminoase. Pe măsură ce flacăra se mișcă de-a lungul fitilului, ceara se topește și trosnește, rupându-se în particule minuscule de carbon. ( Cărbune constă și din carbon.) Aceste particule sunt purtate de flacără în sus și ard. Sunt foarte fierbinți și strălucesc ca spirala plăcii tale. Dar particulele de carbon sunt mult mai fierbinți decât spiralele celei mai fierbinți plăci (temperatura de ardere a carbonului este de aproximativ 1.400 de grade Celsius). Prin urmare, strălucirea lor este galbenă. Lângă fitilul care arde, flacăra este încă mai fierbinte și strălucește albastru.
Flacăra unui șemineu sau a unui foc de tabără are în mare parte un aspect variat. Lemnul arde la o temperatură mai scăzută decât fitilul lumânării, așa că culoarea principală a focului este portocaliu, nu galben. Unele dintre particulele de carbon din foc sunt destul de fierbinți. Sunt puține, dar adaugă o tentă gălbuie la flacără. Particulele răcite de carbon incandescent sunt funingine care se depune cosuri de fum... Temperatura de ardere a lemnului este mai mică decât temperatura de ardere a lumânării. Calciu, sodiu și cupru, încălzite la o temperatură ridicată, strălucesc în diferite culori. Ele sunt adăugate la praful de pușcă al rachetelor pentru a colora luminile artificiilor de sărbători.
Culoarea flăcării și compoziția chimică
Culoarea flăcării se poate schimba în funcție de impuritățile chimice conținute în bușteni sau alte substanțe inflamabile. Flacăra poate conține, de exemplu, impurități de sodiu.

Chiar și în cele mai vechi timpuri, oamenii de știință și alchimiștii au încercat să înțeleagă ce fel de substanțe ard în foc, în funcție de culoarea focului.
- Sodiul este componentă sare de masă. Dacă sodiul este încălzit, acesta devine galben strălucitor.
- Calciul poate intra în foc. Știm cu toții că laptele conține mult calciu. Este metal. Calciul fierbinte devine roșu aprins.
- Dacă fosforul arde în foc, flacăra va deveni verzuie. Toate aceste elemente fie sunt conținute în lemn, fie merg la foc cu alte substanțe.
- Aproape toate casele au sobe pe gaz sau încălzitoare de apă cu flăcări albastre. Acest lucru se datorează carbonului combustibil, monoxid de carbon, care dă această nuanță.

Amestecarea culorilor flăcării, ca și amestecarea culorilor curcubeului, poate produce alb, astfel încât pete albe sunt vizibile în flăcările unui foc de tabără sau șemineu.
Temperatura flăcării în timpul arderii unor substanțe:
Cum să obțineți o culoare uniformă a flăcării?
Pentru a studia mineralele și a determina compoziția lor, se folosește arzător Bunsen, care dă o culoare a flăcării chiar incoloră, care nu interferează cu cursul experimentului, inventat de Bunsen la mijlocul secolului al XIX-lea.

Bunsen era un admirator înflăcărat al elementului foc, deseori lăudându-se cu flăcările. Suflarea sticlei era hobby-ul lui. Sufland diverse modele și mecanisme viclene din sticlă, Bunsen nu a putut observa durerea. S-a întâmplat că degetele lui noduroase au început să fumeze din paharul moale încă fierbinte, dar nu i-a dat atenție. Dacă durerea a depășit deja pragul sensibilității, atunci s-a salvat prin propria sa metodă - și-a apăsat lobul urechii cu degetele, întrerupând o durere cu alta.
El a fost fondatorul metodei de determinare a compoziției unei substanțe după culoarea flăcării. Desigur, înaintea lui, oamenii de știință au încercat să organizeze astfel de experimente, dar nu aveau un arzător Bunsen cu o flacără incoloră care să nu interfereze cu experimentul. A injectat în flacăra arzătorului diverse elemente pe sârmă de platină, deoarece platina nu afectează culoarea flăcării și nu o vopsește.
S-ar părea că metoda este bună, nu este nevoie de analize chimice complexe, a adus elementul la flacără - iar compoziția sa este imediat vizibilă. Dar nu era acolo. Foarte rar, substanțele se găsesc în mod natural în formă pură ele conțin de obicei o mare varietate de impurități care schimbă culoarea.
Bunsen a încercat metode diferite izolarea culorilor si a nuantelor acestora. De exemplu, am încercat să mă uit prin sticlă colorată. Să spunem, sticla albastră stinge culoarea galbenă pe care o dau cele mai comune săruri de sodiu și ai putea distinge purpuriu sau purpuriu. nuanță liliac element nativ. Dar chiar și cu ajutorul acestor trucuri, a fost posibil să se determine compoziția unui mineral complex doar o dată din o sută.
Este interesant! Datorită proprietății atomilor și moleculelor de a emite lumină o anumită culoare a fost dezvoltată o metodă de determinare a compoziției substanțelor, care se numește analiza spectrală... Oamenii de știință studiază spectrul pe care îl emite o substanță, de exemplu, atunci când arde, îl compară cu spectrele elementelor cunoscute și, astfel, îi determină compoziția.

Un experiment științific foarte frumos de la profesorul Nicolas " Flacără colorată„Să luăm flacăra celor patru Culori diferite folosind legile chimiei pentru aceasta.
Setul este foarte interesant, chiar am văzut destul de flacără, o priveliște uimitoare! Interesant pentru toata lumea: atat adulti cat si copii, asa ca il recomand cu drag! Plusul este că această experiență cu focul poate fi efectuată acasă, nu este necesar să ieși afară. Setul conține căni-boluri în care arde o tabletă de combustibil uscat, totul este în siguranță și mai departe podea de lemn(sau masa) pot fi livrate.
Este mai bine, desigur, să desfășurați experiența sub supravegherea adulților. Chiar dacă copiii sunt deja destul de mari. Focul este încă un lucru periculos, dar în același timp... înfiorător (aici acest cuvânt se potrivește foarte bine!) Interesant !! :-))
Vezi fotografia ambalajului kit-ului din galeria de la finalul articolului.
Setul Flacără colorată conține tot ce aveți nevoie pentru a vă desfășura experimentul. Setul include:
- Iodură de potasiu,
- clorura de calciu,
- soluție de acid clorhidric 10%,
- sulfat de cupru,
- fir nicrom,
- sârmă de cupru,
- clorura de sodiu,
- combustibil uscat, cupă de evaporare.
Singurul lucru pe care îl am câteva plângeri la adresa producătorului este că mă așteptam să găsesc o mini-broșură cu o descriere în cutie. proces chimic pe care le vedem aici și o explicație a motivului pentru care flacăra devine colorată. Nu a existat o astfel de descriere aici, așa că trebuie să vă referiți la enciclopedia chimiei (). Dacă, desigur, există o astfel de dorință. Și dorința de copii mai mari, desigur, apare! Copiii mai mici, desigur, nu au nevoie de explicații: pur și simplu sunt foarte interesați să vadă cum se schimbă culoarea flăcării.
Pe spatele cutiei de ambalaj este scris ce trebuie făcut pentru a colora flacăra. La început au făcut-o conform instrucțiunilor, iar apoi doar au stropit flacăra cu diferite pulberi din borcane (când s-au convins că totul este în siguranță) :-)) - efectul este uimitor. :-) Sclipiri de flacără roșie în galben, flacără verde deschis strălucitor, verde, violet... spectacolul este pur și simplu fascinant.
Este foarte tare de cumpărat pentru orice vacanță, este mult mai interesant decât oricare petarde. Și pe Anul Nou va fi foarte tare. Am ars ziua, pe întuneric ar fi și mai spectaculos.
Mai avem reactivi după arderea unei tablete, așa că dacă luați o altă tabletă (cumpărați separat), puteți repeta experimentul. Paharul de lut s-a spălat destul de bine, așa că va fi suficient pentru multe experimente. Și dacă sunteți la dacha, atunci pulberea poate fi stropită și pe focul din foc - atunci, desigur, se va termina repede, dar spectacolul va fi fantastic!
Adăuga informatie scurta despre reactivii care vin odată cu experiența. Pentru copiii curioși care sunt interesați să învețe mai multe. :-)
Colorare cu flacără
Metoda standard de vopsire a unei flăcări de gaz slab luminoase este introducerea de compuși metalici în ea sub formă de săruri volatile (de obicei nitrați sau cloruri):
galben - sodiu,
roșu - stronțiu, calciu,
verde - cesiu (sau bor, sub formă de bor etil sau bor metil eter),
albastru - cupru (sub formă de clorură).
Seleniul colorează flacăra în albastru, iar borul în albastru-verde.
Temperatura din interiorul flăcării este diferită și în timp se modifică (în funcție de fluxul de oxigen și de o substanță combustibilă). Culoarea albastră înseamnă că temperatura este foarte ridicată până la 1400 C, galben - temperatura este puțin mai mică decât atunci când este flacăra albastră. Culoarea flăcării poate varia în funcție de impuritățile chimice.
Culoarea unei flăcări este determinată doar de temperatura acesteia, dacă nu se ține cont de compoziția sa chimică (mai precis, elementară). niste elemente chimice sunt capabili să coloreze flacăra într-o culoare caracteristică acestui element.
În condiții de laborator, se poate obține un foc complet incolor, care poate fi determinat doar de vibrația aerului din zona de ardere. Focul menajer este întotdeauna „colorat”. Culoarea focului este determinată de temperatura flăcării și de ce substanțe chimice ard în ea. Căldură flacăra permite atomilor să sară pentru un timp într-o stare de energie mai mare. Când atomii revin la starea lor inițială, ei emit lumină la o anumită lungime de undă. Corespunde structurii carcaselor electronice ale acestui element.
Galbăstrui flacăra, de exemplu, care se vede la arderea gazelor naturale, este cauzată de monoxidul de carbon, care conferă flăcării această nuanță. Monoxid de carbon, a cărei moleculă este formată dintr-un atom de oxigen și un atom de carbon, este un produs secundar al arderii gazelor naturale.
Potasiu - flacăra violetă
1) B verde Culoare flacără vopsele borice acid sau fir de cupru (alamă) înfipt ser fiziologic acid.
2) În roșu flacără pete de cretă înmuiate în același ser fiziologic acid.
Când sunt puternic calcinate în fragmente subțiri, mineralele care conțin Ba (conțin bariu) colorează flacăra într-o culoare galben-verde. Colorarea flăcării poate fi sporită dacă, după calcinare preliminară, mineralul este umezit în acid clorhidric puternic.
Oxizi de cupru (în experimentul pentru o flacără verde se folosesc acid clorhidric și cristale de cupru) da o culoare verde smarald. Compușii cu conținut de Cu calcinat umeziți cu HC1 colorează flacăra în culoarea albastru azur CuCl 2). Reacția este foarte sensibilă.
Bariul, molibdenul, fosforul, antimoniul dau, de asemenea, culoarea verde și nuanțele sale la foc.
Soluțiile de acid azotic și acid clorhidric de cupru sunt albastre sau verzi; adăugarea de amoniac schimbă culoarea soluției în albastru închis.
Flacără galbenă - sare
Pentru galben flacără este necesar un aditiv alimentar sare, azotat de sodiu sau cromat de sodiu.
Încercați să stropiți pe plită aragaz cu o flacără albastră transparentă, puțină sare de masă - vor apărea limbi galbene în flacără. Astfel de flacără galben-portocalie dați săruri de sodiu (a sare, amintiți-vă, aceasta este clorură de sodiu).
Culoarea galbenă este culoarea sodiului din flacără. Sodiul se găsește în orice material organic natural, motiv pentru care de obicei vedem flacăra ca fiind galbenă. Și galbenul este capabil să înece alte culori - aceasta este o caracteristică a vederii umane.
Flăcări galbene apar atunci când sărurile de sodiu se descompun. Lemnul este foarte bogat în astfel de săruri, așa că un incendiu de pădure obișnuit sau chibriturile de uz casnic ard cu o flacără galbenă.
Temperatura focului te face să vezi lucruri familiare într-o lumină nouă - un chibrit strălucit în alb, o strălucire albastră a unui arzător aragazîn bucătărie, limbi roșii-portocalii deasupra unui copac care arde. O persoană nu acordă atenție focului până când vârfurile degetelor îi sunt arse. Sau nu va arde cartofii în tigaie. Sau nu va arde prin tălpile pantofilor sport care se usucă la foc.
Când trec prima durere, teamă și dezamăgire, vine momentul reflecției filozofice. Despre natura, culorile, temperatura focului.
Arde ca un chibrit
Pe scurt despre structura meciului. Este format dintr-un băț și un cap. Bastoanele sunt realizate din lemn, carton și câlți de bumbac impregnat cu parafină. Arborele este ales specii moi - plop, pin, aspen. Materiile prime pentru bețe se numesc bețișoare de chibrit. Pentru a evita paiele care mocnesc, bastoanele sunt impregnate cu acid fosforic. Fabricile rusești fac paie de aspen.
Capul unui chibrit este simplu ca formă, dar complex ca compoziție chimică. Capul maro închis al chibritului conține șapte componente: agenți oxidanți - sare de berthollet și dicromat de potasiu; praf de sticlă, plumb roșu, sulf, alb de zinc.

Capul unui chibrit se aprinde în timpul frecării, încălzindu-se până la o mie și jumătate de grade. Pragul de inflamabilitate, în grade Celsius:
- plop - 468;
- aspen - 612;
- pin - 624.
Temperatura focului chibritului este egală cu temperatura Prin urmare, fulgerul alb al capului de sulf este înlocuit cu limba galben-portocalie a chibritului.
Dacă te uiți cu atenție la un chibrit care arde, atunci apar trei zone de flacără. Cel de jos este albastru rece. Media este de o ori și jumătate mai caldă. Partea de sus este zona fierbinte.
Artist înflăcărat
La cuvântul „foc” se aprind amintiri nu mai puțin nostalgice: fumul focului, creând o atmosferă confidențială; roşu şi lumini galbene zburând spre cerul ultramarin; joc de stuf de la albastru la roșu rubin; cărbuni de răcire purpuriu în care se coc cartofii „pionier”.
Schimbarea culorii lemnului care arde indică fluctuații ale temperaturii focului în foc. Mocnirea (întunecarea) a lemnului începe la 150 °. Aprinderea (fumul) are loc în intervalul 250-300 °. Cu aceeași aprovizionare cu oxigen la rocă la temperaturi nepotrivite. În consecință, și gradul de incendiu va fi diferit. Mesteacanul arde la 800 de grade, arinul la 522 de grade, iar frasinul și fagul la 1040 de grade.

Dar culoarea focului este determinată și de compoziția chimică a substanței care arde. Galbenul și portocaliul contribuie cu săruri de sodiu. Compoziție chimică celuloza conține atât săruri de sodiu, cât și săruri de potasiu, care conferă cărbunilor strălucitori ai lemnului o nuanță roșie. Romantismul într-un foc de lemne apare din cauza lipsei de oxigen, când în loc de CO 2 se formează CO - monoxid de carbon.
Pasionații de știință măsoară temperatura unui foc într-un foc de tabără cu un instrument numit pirometru. Sunt produse trei tipuri de pirometre: optice, cu radiații, spectrale. Acestea sunt dispozitive fără contact care permit evaluarea puterii radiației termice.
Explorând focul în propria noastră bucătărie
Sobele pe gaz funcționează cu două tipuri de combustibil:
- Coloana vertebrală gaz natural metan.
- Amestec lichefiat propan-butan din butelii și rezervoare de gaz.
Compoziția chimică a combustibilului determină temperatura focului sobei cu gaz. Metanul, arzând, formează un foc cu o capacitate de 900 de grade în punctul cel mai înalt.
Arderea unui amestec lichefiat dă căldură până la 1950 °.
Un observator atent va observa colorarea neuniformă a limbilor arzătorului aragazului cu gaz. În interiorul torței de foc, există o împărțire în trei zone:
- Zonă întunecată situată în apropierea arzătorului: nu există ardere aici din cauza lipsei de oxigen, iar temperatura zonei este de 350 °.
- O zonă luminoasă situată în centrul torței: gazul care arde se încălzește până la 700 °, dar combustibilul nu arde complet din cauza lipsei unui oxidant.
- Secțiunea superioară semi-transparentă: atinge 900 ° C și arderea completă a gazului.
Numerele zonele de temperatură pentru metan se dau torțe cu flacără.
Reguli de securitate la incendiu
Când aprindeți chibrituri, aragaz, aveți grijă de aerisirea încăperii. Asigurați alimentarea cu oxigen a combustibilului.
Nu încercați să vă reparați singur echipamente de gaz... Gazul nu tolerează amatorii.

Gospodinele notează că arzătoarele aprind in albastru dar uneori focul devine portocaliu. Aceasta nu este o schimbare globală a temperaturii. Schimbarea culorii este asociată cu o modificare a compoziției combustibilului. Metanul pur arde incolor și inodor. Din motive de securitate în gaz de uz casnic adăugați sulf, care, atunci când este ars, colorează gazul nuanțe de albastruși conferă un miros caracteristic produselor de ardere.
Apariția nuanțelor portocalii și galbene în focul arzătorului indică necesitatea manipulărilor preventive cu aragazul. Meșterii vor curăța echipamentul, vor îndepărta praful și funinginea, a căror ardere schimbă culoarea obișnuită a focului.
Uneori, focul din arzător devine roșu. Acesta este un semnal al unui conținut periculos de monoxid de carbon în alimentarea cu oxigen a combustibilului este atât de mică încât aragazul se stinge chiar. Monoxidul de carbon este fără gust și inodor, iar o persoană aflată în apropierea sursei de emisie a unei substanțe nocive va observa prea târziu că a fost otrăvită. Prin urmare, culoarea roșie a gazului necesită o chemare imediată a maiștrilor pentru prevenirea și reglarea echipamentului.